白条怎么自己套出来?亲身检测白条真的能取现吗?
| 该疗法名为 NTLA-2001,由美国生物技术公司 Intellia Therapeutics 和 Regeneron(再生元)联合研发,用于治疗转甲状腺素蛋白淀粉样变性(ATTR)患者。 提现服务联系图片中客服QQ 咨询电话18052232749
研究结果显示,NTLA-2001 治疗后,0.1 mg/kg 剂量组患者血清TTR 下降 52%, 0.3 mg/kg 剂量组下降 87%,两个剂量组患者耐受钧良好,暂未出现严重不良事件和肝脏损害,该疗法显示出良好的有效性和安全性[1]。 此消息一出,很快引起广泛关注,医疗界不乏溢美之词,嗅觉一向灵敏的资本市场也快速反应,研发公司的股价相应大涨了一波。 应用基因编辑技术治疗人类遗传病的梦想,就要照进现实了吗? 为什么可以用 CRISPR 治疗 ATTR? ATTR 是一种罕见却足以致命的疾病,其发病机制与转胸腺素(TTR)基因异常有关。 正常的 TTR 蛋白主要在肝脏中合成,在正常生理条件下,TTR 蛋白以同源四聚体形式存在于外周血中,是甲状腺素和视黄醇结合蛋白的转运蛋白。 TTR 基因异常导致 TTR 四聚体解离成低构象稳定性的非天然单体,随后单体发生错误折叠,形成淀粉样蛋白,进而聚集形成不溶性淀粉样蛋白原纤维,在外周神经系统、心脏、眼、肾脏、脑膜等组织沉积,导致进行性感觉运动多神经病变和自主神经功能障碍[2],具体临床表现包括进行性痴呆、共济失调、癫痫发作等。未经治疗的患者平均寿命只有短短 10 年,在此期间,患者的神经功能还会逐年恶化,最后因心脏受累而死[3]。 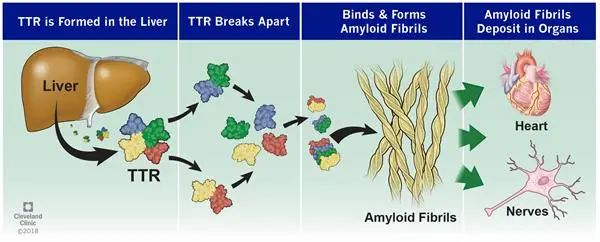 ATTR的发病机制 图源:Cleveland Clinic 多年来,ATTR 唯一的药物治疗方法是非甾体类抗炎药二氟尼柳。2018 年,Onpattro、 Tegsedi 和 Vyndamax 三种新药获得 FDA 批准,但这三种新药并不能治愈 ATTR,只能缓解疾病症状,且价格高昂(每年花费约 22~45 万美元)[4]、必须终身服用,还可能存在肾功能损害和凝血功能减弱等副作用。 唯一可能治愈 ATTR 的方法是肝移植,它可以消除血液循环中致病性 TTR 蛋白的主要来源。考虑到患者肝移植后有发生进行性心肌病的风险,患者往往需要进行心肝联合移植,移植费用与风险可见一斑。 在这样的背景下,Intellia Therapeutics 公司的 NTLA-2001 在今年 3 月被欧盟委员会(EC)授予孤儿药称号[5],即罕见病用药。孤儿药资格授予旨在治疗、预防或诊断危及生命或慢性加重的罕见疾病疗法,这些疾病要么没有治疗方法,要么没有令人满意的治疗选择。 其实在 ATTR 之外,还有两种疾病在这家公司基因治疗体内途径的研发候选名单上:遗传性血管性水肿、血友病[6],最终 ATTR 能够率先抢跑,和公司此前的研究进度有关。 2017 年,Intellia Therapeutics 研发出脂质纳米颗粒 (LNP) 递送系统,当时的研究对象正是 ATTR,这项技术也成了本次基因治疗的基础。 在进行体内治疗的过程中,脂质纳米颗粒递送系统就像包饺子——脂质纳米颗粒是「饺子皮」,其中包裹着有效的治疗成分「饺子馅」。通过静脉给药,将基因编辑系统安全递送至患者肝脏内,包括识别致病基因的引导 RNA(即 CRISPR)和编码 Cas9 酶的 RNA,从而特异性敲除肝脏细胞中的 TTR 基因,阻止错误折叠的 TTR 产生。 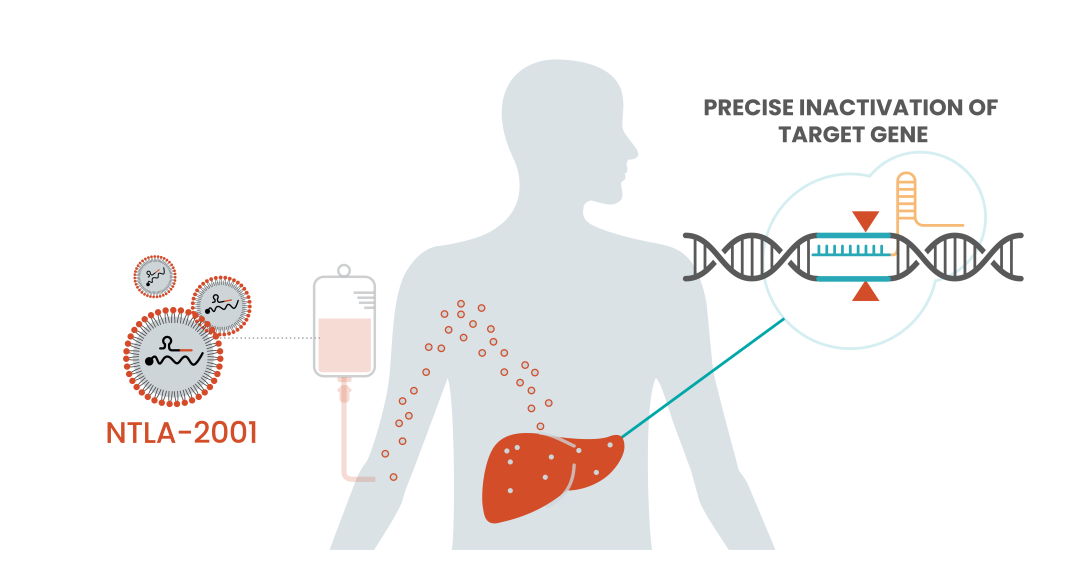 NTLA-2001药物的作用机制 图源:智能疗法公司官网 小鼠研究表明:单次给药后,小鼠血清 TTR 蛋白水平降低约 97%,效果持续一年;小鼠肝脏内约 70% 目标 DNA 位点完成编辑 [7]。在此基础上,Intellia Therapeutics 开启本次 I 期临床试验。 该研究计划招募 38 名成年患者,目前所出的前 6 名患者的结果显示,NTLA-2001 治疗后,0.1 mg/kg 剂量组患者血清 TTR 下降 52%, 0.3 mg/kg 剂量组下降 87%(其中一名患者下降 96%),两个剂量组患者耐受钧良好,暂未出现严重不良事件和肝脏损害,表现出良好的有效性和安全性。 目前,该试验将继续增加治疗剂量评估效果,截至 6 月26 日,第 3 个单递增剂量队列(1 mg/kg)患者正在登记中[8]。 「首个」称号背后的专利之争 Intellia Therapeutics 能在竞争激烈基因编辑治疗赛道上拔得头筹,离不开其得天独厚的优势——专利。公司创始人之一道德纳,正是在 2012 年分离了 CRISPR-Cas9 并使它在试管中发挥作用、从而获得 2020 年诺贝尔化学奖的两位科学家之一。  2020 诺贝尔化学奖 图源:诺贝尔奖官网 2011年,科学家沙尔庞捷在对化脓性链球菌进行研究期间,发现 CRISPR/Cas9 作为细菌的免疫系统,可以切割病毒的 DNA,从而抵抗病毒入侵。同年,沙尔庞捷开始与道德纳合作,成功在试管中制造出基因剪刀 CRISPR/Cas9,并对它进行重新编程,实现在指定位点切割 DNA。 随着这一发现在 2012 年见刊 Science,CRISPR 领域很快受到世界瞩目,大量科研力量投身这一领域,各种研究成果层出不穷。2020 年,两人共同获得诺贝尔化学奖[9]。 虽然道德纳和沙尔庞捷最先发现基因剪刀,首次将基因剪刀应用于哺乳动物的则是华人科学家张锋。打个比方,道德纳和沙尔庞捷最先发现了基因编辑技术这座金矿,而张锋则最先找到了这座金矿中的金子。 |

 支付宝扫一扫
支付宝扫一扫 微信扫一扫
微信扫一扫









评论列表